Ερευνητές του Πανεπιστημίου Northwestern ανέπτυξαν ένα νέο αντιοξειδωτικό βιοϋλικό που κάποια μέρα θα μπορούσε να προσφέρει την απαραίτητη ανακούφιση σε άτομα που ζουν με χρόνια παγκρεατίτιδα.
Η εργασία, “Phase-changing citrate macromolecule combats oxidative pancreatic islet damage, enables islet engraftment and function in the omentum”, δημοσιεύθηκε στις 7 Ιουνίου στο περιοδικό Science Advances.
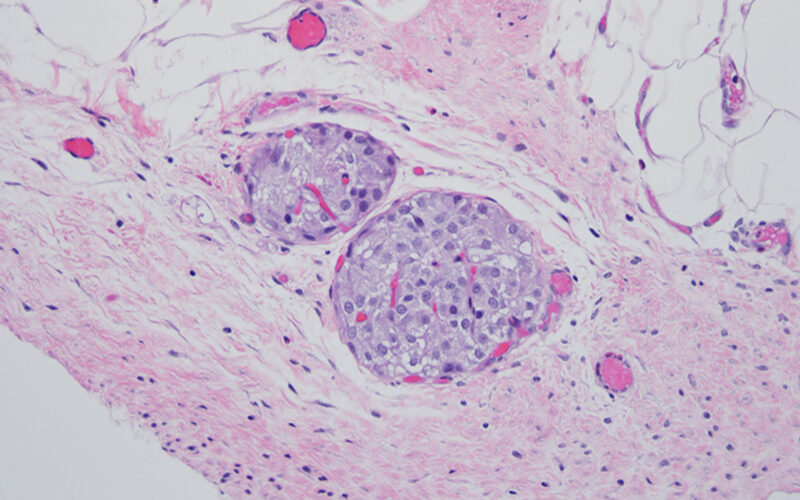
Προτού οι χειρουργοί αφαιρέσουν το πάγκρεας από ασθενείς με σοβαρή, επώδυνη χρόνια παγκρεατίτιδα, συλλέγουν πρώτα ομάδες ιστών που παράγουν ινσουλίνη, που ονομάζονται νησίδες, και τις μεταμοσχεύουν στο αγγείο του ήπατος. Ο στόχος της μεταμόσχευσης είναι να διατηρήσει την ικανότητα του ασθενούς να ελέγχει τα δικά του επίπεδα γλυκόζης στο αίμα χωρίς ενέσεις ινσουλίνης.
Δυστυχώς, η διαδικασία καταστρέφει ακούσια το 50-80% των νησίδων και το ένα τρίτο των ασθενών γίνονται διαβητικοί μετά την επέμβαση. Τρία χρόνια μετά την επέμβαση, το 70% των ασθενών χρειάζονται ενέσεις ινσουλίνης, οι οποίες συνοδεύονται από μια λίστα παρενεργειών, συμπεριλαμβανομένης της αύξησης βάρους, της υπογλυκαιμίας και της κόπωσης.
Στη νέα μελέτη, οι ερευνητές μεταμόσχευσαν νησίδες από το πάγκρεας στο στόμιο –τον μεγάλο, επίπεδο, λιπώδη ιστό που καλύπτει τα έντερα– αντί του ήπατος. Και, για να δημιουργήσουν ένα πιο υγιές μικροπεριβάλλον για τις νησίδες, οι ερευνητές προσκόλλησαν τις νησίδες στο στόμιο με ένα εγγενές αντιοξειδωτικό και αντιφλεγμονώδες βιοϋλικό, το οποίο μετατρέπεται γρήγορα από υγρό σε gel όταν εκτίθεται στη θερμοκρασία του σώματος.
Σε μελέτες με πρωτεύοντα ποντίκια και πλην του ανθρώπου, το τζελ απέτρεψε με επιτυχία το οξειδωτικό στρες και τις φλεγμονώδεις αντιδράσεις, βελτιώνοντας σημαντικά την επιβίωση και διατηρώντας τη λειτουργία των μεταμοσχευμένων νησίδων. Σηματοδοτεί την πρώτη φορά που χρησιμοποιείται ένα συνθετικό αντιοξειδωτικό τζελ για τη διατήρηση της λειτουργίας των μεταμοσχευμένων νησίδων.
«Αν και η μεταμόσχευση νησίδων έχει βελτιωθεί με τα χρόνια, τα μακροπρόθεσμα αποτελέσματα παραμένουν φτωχά», δήλωσε ο Guillermo A. Ameer του Northwestern, ο οποίος ηγήθηκε της μελέτης.
«Υπάρχει ξεκάθαρα ανάγκη για εναλλακτικές λύσεις. Κατασκευάσαμε ένα συνθετικό υλικό αιχμής που παρέχει ένα υποστηρικτικό μικροπεριβάλλον για τη λειτουργία των νησιδίων. Όταν δοκιμάσαμε σε ζώα, ήμασταν επιτυχείς. Διατήρησε τη λειτουργία των νησιδίων μεγιστοποιημένη και αποκατέστησε τα φυσιολογικά επίπεδα σακχάρου στο αίμα. Παρατηρήσαμε επίσης μείωση των μονάδων ινσουλίνης που χρειάζονταν τα ζώα».
«Με αυτή τη νέα προσέγγιση, ελπίζουμε ότι οι ασθενείς δεν θα χρειάζεται πλέον να επιλέγουν μεταξύ του σωματικού πόνου της χρόνιας παγκρεατίτιδας ή των επιπλοκών του διαβήτη», πρόσθεσε η Jacqueline Burke, επίκουρη καθηγήτρια βιοϊατρικής μηχανικής στο Northwestern και η πρώτη συγγραφέας της εργασίας.
Ζωή χωρίς συμβιβασμούς
Για τους ασθενείς που ζουν χωρίς πάγκρεας, οι παρενέργειες όπως η διαχείριση των επιπέδων σακχάρου στο αίμα μπορεί να είναι μια δια βίου μάχη. Εκκρίνοντας ινσουλίνη ως απόκριση στη γλυκόζη, οι νησίδες βοηθούν το σώμα να διατηρήσει τον γλυκαιμικό έλεγχο. Χωρίς λειτουργικές νησίδες, οι άνθρωποι πρέπει να παρακολουθούν στενά τα επίπεδα σακχάρου στο αίμα τους και να κάνουν συχνά ένεση ινσουλίνης.
«Η ζωή χωρίς λειτουργικές νησίδες επιβαρύνει πολύ τους ασθενείς», είπε η Burke. «Πρέπει να μάθουν να μετρούν τους υδατάνθρακες, να λαμβάνουν δόση ινσουλίνης την κατάλληλη στιγμή και να παρακολουθούν συνεχώς τη γλυκόζη του αίματος. Αυτό καταναλώνει μεγάλο μέρος του χρόνου και της ψυχικής τους ενέργειας.
Ακόμη και με μεγάλη προσοχή, η εξωγενής θεραπεία ινσουλίνης δεν είναι τόσο αποτελεσματική όσο οι νησίδες για τη διατήρηση του ελέγχου της γλυκόζης. Οι ασθενείς με επίπεδα γλυκόζης στο αίμα εκτός εύρους θα εμφανίσουν επιπλοκές, όπως τύφλωση και ακρωτηριασμό. Στόχος μας είναι αυτό το βιοϋλικό να διατηρήσει τις νησίδες, ώστε οι ασθενείς να μπορούν να ζήσουν μια φυσιολογική ζωή – μια ζωή χωρίς διαβήτη».
«Αντί για πολλαπλές ενέσεις ινσουλίνης, θα θέλαμε να συλλέξουμε και να διατηρήσουμε όσο το δυνατόν περισσότερες νησίδες» είπε ο Ameer, ως ειδικός στην αναγεννητική μηχανική.
Όμως, δυστυχώς, το τρέχον πρότυπο φροντίδας για τη διατήρηση των νησίδων συχνά οδηγεί σε κακά αποτελέσματα. Μετά την επέμβαση αφαίρεσης του παγκρέατος, οι χειρουργοί απομονώνουν νησίδες από το πάγκρεας και τις μεταμοσχεύουν στο ήπαρ μέσω έγχυσης της πυλαίας φλέβας.
Αυτή η διαδικασία αιμάτωσης έχει αρκετές κοινές επιπλοκές. Οι νησίδες που έρχονται σε άμεση επαφή με τη ροή του αίματος υφίστανται μια φλεγμονώδη απόκριση, περισσότερες από τις μισές νησίδες πεθαίνουν και οι μεταμοσχευμένες νησίδες μπορούν να προκαλέσουν επικίνδυνους θρόμβους στο ήπαρ. Για αυτούς τους λόγους, γιατροί και ερευνητές αναζητούν μια εναλλακτική τοποθεσία μεταμόσχευσης.
Σε προηγούμενες κλινικές μελέτες, οι ερευνητές μεταμόσχευσαν νησίδες στο οπίσθιο αντί για το ήπαρ, προκειμένου να παρακάμψουν προβλήματα με την πήξη. Για να ασφαλίσουν τις νησίδες πάνω στο στόμιο, οι γιατροί χρησιμοποίησαν πλάσμα από το ίδιο το αίμα των ασθενών για να σχηματίσουν μια βιολογική γέλη. Ενώ το στόμιο φαινόταν να λειτουργεί καλύτερα από το συκώτι ως σημείο μεταμόσχευσης, πολλά προβλήματα, συμπεριλαμβανομένων των θρόμβων και της φλεγμονής, παρέμειναν.
«Υπήρξε σημαντικό ενδιαφέρον στις ερευνητικές και ιατρικές κοινότητες να βρουν μια εναλλακτική τοποθεσία μεταμόσχευσης νησίδων», είπε ο Ameer. «Τα αποτελέσματα από τη μελέτη στο στόμιο ήταν ενθαρρυντικά, αλλά τα αποτελέσματα ήταν ποικίλα. Πιστεύουμε ότι αυτό οφείλεται στο ότι η χρήση του αίματος των ασθενών και των πρόσθετων συστατικών που απαιτούνται για τη δημιουργία του βιολογικού τζελ μπορεί να επηρεάσει την αναπαραγωγιμότητα μεταξύ των ασθενών.»
Ένα κιτρικό διάλυμα
Για να προστατεύσει τις νησίδες και να βελτιώσει τα αποτελέσματα, ο Ameer στράφηκε στην πλατφόρμα βιοϋλικών με βάση το κιτρικό άλας με εγγενείς αντιοξειδωτικές ιδιότητες που αναπτύχθηκαν στο εργαστήριό του. Χρησιμοποιούνται σε προϊόντα εγκεκριμένα από τον Οργανισμό Τροφίμων και Φαρμάκων των ΗΠΑ για μυοσκελετικές επεμβάσεις, τα βιοϋλικά με βάση το κιτρικό έχουν αποδείξει την ικανότητα ελέγχου των φλεγμονωδών αποκρίσεων του σώματος. Ο Ameer ξεκίνησε να διερευνήσει εάν μια έκδοση αυτών των βιοϋλικών με βιοαποικοδομήσιμες και ανταποκρινόμενες στη θερμοκρασία ιδιότητες αλλαγής φάσης θα παρείχε μια ανώτερη εναλλακτική σε ένα βιολογικό τζελ που λαμβάνεται από αίμα.
Σε καλλιέργειες κυττάρων, τόσο οι νησίδες ποντικού όσο και οι ανθρώπινες νησίδες που ήταν αποθηκευμένες στο τζελ με βάση το κιτρικό διατήρησαν τη βιωσιμότητα πολύ περισσότερο από τις νησίδες σε άλλα διαλύματα. Όταν εκτέθηκαν στη γλυκόζη, οι νησίδες εκκρίνουν ινσουλίνη, επιδεικνύοντας φυσιολογική λειτουργικότητα. Προχωρώντας πέρα από τις κυτταροκαλλιέργειες, η ομάδα του Ameer δοκίμασε το τζελ σε μικρά και μεγάλα ζωικά μοντέλα. Υγρό σε θερμοκρασία δωματίου, το υλικό μετατρέπεται σε τζελ στη θερμοκρασία του σώματος, επομένως είναι απλό στην εφαρμογή του και μένει εύκολα στη θέση του.
Στις μελέτες σε ζώα, το τζελ ασφάλισε αποτελεσματικά τις νησίδες πάνω στο μάτι των ζώων. Σε σύγκριση με τις τρέχουσες μεθόδους, περισσότερες νησίδες επέζησαν και, με την πάροδο του χρόνου, τα ζώα αποκατέστησαν τα φυσιολογικά επίπεδα γλυκόζης στο αίμα. Σύμφωνα με τον Ameer, η επιτυχία οφείλεται εν μέρει στη βιοσυμβατότητα του νέου υλικού και στην αντιοξειδωτική φύση του.
«Οι νησίδες είναι πολύ ευαίσθητες στο οξυγόνο», εξήγησε ο Ameer. «Επηρεάζονται τόσο από πολύ λίγο οξυγόνο όσο και από πολύ οξυγόνο. Οι έμφυτες αντιοξειδωτικές ιδιότητες του υλικού προστατεύουν τα κύτταρα. Το πλάσμα από το αίμα σας δεν προσφέρει το ίδιο επίπεδο προστασίας».
Ενσωμάτωση στους ιστούς
Μετά από περίπου τρεις μήνες, το σώμα απορρόφησε το 80-90% του βιοσυμβατού τζελ. Όμως, σε εκείνο το σημείο, δεν χρειαζόταν πλέον.
«Αυτό που ήταν συναρπαστικό είναι ότι οι νησίδες αναγέννησαν τα αιμοφόρα αγγεία», είπε ο Ameer. «Το σώμα δημιούργησε ένα δίκτυο νέων αιμοφόρων αγγείων για να επανασυνδέσει τις νησίδες με το σώμα. Αυτή είναι μια σημαντική ανακάλυψη επειδή τα αιμοφόρα αγγεία διατηρούν τις νησίδες ζωντανές και υγιείς. Εν τω μεταξύ, το τζελ μας απλώς απορροφάται στον περιβάλλοντα ιστό, αφήνοντας λίγα στοιχεία πίσω».
Στη συνέχεια, ο Ameer στοχεύει να δοκιμάσει την υδρογέλη του σε ζωικά μοντέλα για μεγαλύτερο χρονικό διάστημα. Είπε ότι η νέα υδρογέλη θα μπορούσε επίσης να χρησιμοποιηθεί για διάφορες θεραπείες αντικατάστασης κυττάρων, συμπεριλαμβανομένων των βήτα κυττάρων που προέρχονται από βλαστοκύτταρα για τη θεραπεία του διαβήτη.